ความรู้ทั่วไปเกี่ยวกับเหล็กชุบเคลือบสังกะสี
เป็นที่ทราบกันดีว่าเหล็ก และเหล็กกล้าเกิดสนิมได้ง่ายหากวางทิ้งไว้ใน บรรยากาศ สนิมเป็นออกไซด์ของเหล็กที่เกิดจากปฏิกิริยาระหว่างออกซิเจน กับเนื้อเหล็ก ดังนั้นวิธีหนึ่งที่ใช้ป้องกันเหล็กไม่ให้เกิดสนิม คือ การเคลือบสารปิดทับผิวเหล็กไว้ สารเคลือบที่ใช้มีด้วยกันหลายชนิด สังกะสีก็เป็นโลหะชนิดหนึ่งที่นิยมนำมาเคลือบ เหล็กที่ได้จากการชุบเคลือบสังกะสีเรียกว่า เหล็กกล้าชุบเคลือบสังกะสี (galvanized steel)
การชุบเคลือบสังกะสีมีด้วยกันหลายวิธี เช่น การชุบเคลือบสังกะสีแบบจุ่มร้อน (hot dip galvanizing) การเคลือบสังกะสีด้วยไฟฟ้า (electrogalvanizing) การเคลือบด้วยวิธีทางกล (mechanical coatings) การพ่นเคลือบด้วยเปลวความร้อน (zinc spraying) การทาด้วยสีฝุ่นสังกะสี (zinc-rich paints) การชุบเคลือบสังกะสีแบบจุ่มร้อนด้วยกระบวนการต่อเนื่อง (continuous hot dip galvanizing) การเคลือบด้วยเทคนิคเชอร์ราไดซ์ซิ่ง (sherardizing) แต่บทความนี้ขอเน้นเฉพาะเรื่องการชุบเคลือบสังกะสีแบบจุ่มร้อน ซึ่งวิธีนี้ถูกนำออกเผยแพร่ครั้งแรกในปี ค.ศ. 1742 โดยนักเคมีชาวฝรั่งเศส P.J. Malouin
การชุบสังกะสีด้วยวิธีจุ่มร้อน(Hot Dip Galvanizing เรียกโดยย่อว่า HDG) หมายถึง การนำชิ้นงานที่ผ่านการทำความสะอาดผิวหน้ามาดีแล้ว และต้องการชุบผิวด้วยสังกะสีไปจุ่มลงในอ่างชุบ (molten zinc bath) ซึ่งบรรจุน้ำสังกะสีอยู่ ในสภาพของเหลวร้อนจัดมีอุณหภูมิขณะใช้งานอยู่ในช่วง 445 ถึง 465 0c (830 ถึง 870 ๐F) สังกะสีจะทำปฏิกริยากับเหล็ก เกิดเป็นชั้นของโลหะผสมเคลือบผิวชิ้นงาน (zinc – iron alloy layers) และเมื่อนำ ชิ้นงานขึ้นจากอ่างชุบสังกะสี และทำให้เย็นตัวลง นํ้าสังกะสีก็จะแห้งกลายเป็นผิวเคลือบหุ้มชิ้นงานเอาไว้
และด้วยการค้นคว้าวิจัยในหลายๆ แง่มุม ของกระบวนการผลิตที่มีมาอย่างต่อเนื่อง ผสานเข้ากับเทคโนโลยีที่ทันสมัยทำให้การชุบสังกะสีเป็นอุตสาหกรรมที่สามารถพัฒนาและควบคุมได้ในทางเทคนิค
โดยทั่วไปสังกะสีเป็นวัสดุที่นิยมนำมาใช้เป็นผิวเคลือบเหล็กมากที่สุด นอกจากนี้ก็มี อะลูมิเนียม, แคดเมียม, ดีบุก, ตะกั่ว, นิกเกิล, ทองเหลือง และทองแดง เป็นต้น
การชุบสังกะสีด้วยวิธีจุ่มร้อนบนชิ้นงานที่เป็นเหล็กกล้าเป็นกระบวนการที่รู้จักกันดีมานานดังกล่าวมาแล้วในตอนต้น ตัวอย่างงานที่ใกล้ตัวเรามากที่สุดก็คือ สังกะสีมุงหลังคาบ้านนั่นเอง
ผิวของสังกะสีจะช่วยเคลือบป้องกัน ผิวหน้าของเหล็กได้อย่างมีประสิทธิภาพ มากกว่าการทาด้วยนํ้ามันหรือทาสีอีกทั้งการทาก็มีขีดจำกัดในบริเวณที่เข้าถึงยาก แต่ถ้าเป็นการชุบสังกะสี
แล้วนํ้าสังกะสีจะไหลไปยังทุกซอกทุกมุมได้ดีกว่า จึงทำให้เหล็กกล้าสามารถทนทานต่อการกัดกร่อน จากสภาวะดินฟ้าอากาศ, ทนทานต่อการถูกฝังไว้ในดินหรือกระทั่งแช่นํ้าทะเล



สังกะสีป้องกันสนิมเหล็กได้อย่างไร?
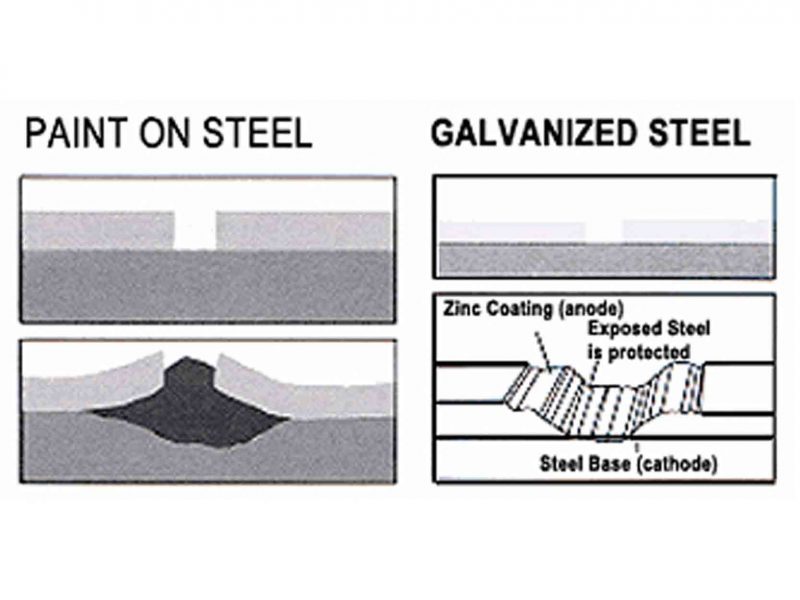
การชุบเคลือบสังกะสีปิดผิวเหล็กทำให้ออกซิเจน ไอน้ำ และโดยเฉพาะอย่างยิ่งคลอไรด์ (chloride) ซึ่งมีฤทธิ์กัดกร่อนเหล็กได้ดี ไม่สามารถสัมผัสและทำปฏิกิริยากับเหล็กได้จึงเป็นการป้องกันระดับหนึ่ง นอกจากนี้ในกรณีที่ผิวเคลือบสังกะสีถูกแรงกระทำ จนเกิดรอยลึกถึงเนื้อเหล็ก แล้ว สังกะสีก็ยังคงสามารถป้องกันเหล็กจากการกัดกร่อนได้ เนื่องจากสังกะสีเป็นโลหะที่มีค่าศักย์ไฟฟ้าต่ำกว่าเหล็ก (ภาพข้างบน) จึงเกิดปฏิกิริยาเคมีได้ง่ายกว่าเหล็ก ลักษณะการใช้โลหะที่มีศักย์ไฟฟ้าต่ำ ร่วมกับโลหะที่มีค่าศักย์ ไฟฟ้าสูงกว่า เพื่อให้โลหะที่มีค่าศักย์ไฟฟ้าต่ำกว่า เกิดปฏิกิริยากัดกร่อนก่อนโลหะที่มี ค่าศักย์ไฟฟ้าสูงเรียกว่า การป้องกันแบบแคโทดิก (cathodic protection)
การนำไปใช้
ผลิตภัณฑ์เหล็กชุบเคลือบสังกะสี สามารถนำไปใช้งานได้ในอุตสาหกรรมหลาย ประเภท ไม่ว่าจะเป็นอุตสาหกรรมยานยนต์ อุตสาหกรรมก่อสร้าง และอุตสาหกรรมอื่น ๆ แต่มีข้อสังเกตอย่างหนึ่ง คือ ชิ้นงานที่เคลือบสังกะสีเป็นชั้นบาง จะไม่เหมาะสำหรับการใช้งานภายนอกอาคาร อย่างเช่น ชิ้นงานที่เคลือบสังกะสีด้วยวิธีเคลือบด้วยไฟฟ้า มีชั้นเคลือบหนาประมาณ 5 – 10 ไมครอน (ไมครอน = 10-6 m) ซึ่งไม่เหมาะกับงานภายนอกอาคาร ขณะที่ชิ้นงานเหล็กที่ชุบเคลือบสังกะสีแบบจุ่มร้อน จะมีชั้นเคลือบสังกะสี หนาตั้งแต่ 65 – 300 ไมครอน ทำให้มีความทนทานต่อการกัดกร่อนจากสภาพแวดล้อม มากกว่าจึงเหมาะกับการใช้งาน ภายนอกอาคารมากกว่า
แหล่งข้อมูลอ้างอิง
บุญรักษ์ กาญจนวรวณิชย์, ศูนย์เทคโนโลยีโลหะและวัสดุแห่งชาติ
วีระศักดิ์ พิรักษา, วารสารเทคนิค 183, เมษายน 2543
วีระศักดิ์ พิรักษา, วารสารเทคนิค 184, พฤษภาคม 2543
http://www.mooregalvanizing.com/galvanizing_coating.htm
http://www.azom.com/details.asp?ArticleID=2629
http://www.galvanizeit.org/
http://en.wikipedia.org/wiki/Galvanize
http://www.mooregalvanizing.com/galvanizing_performance.htm
http://www.zincinfocentre.org/zinc_applications.html#coatings
http://www.mooregalvanizing.com/galvanizing_performance.htm


What Is Galvanized Steel?
Galvanized steel is steel that has gone through a chemical process to keep it from corroding. The steel gets coated in layers of zinc oxide because this protective metal does not get rusty as easily. The coating also gives the steel a more durable, hard to scratch finish that many people find attractive. For countless outdoor, marine, or industrial applications, galvanized steel is an essential fabrication component.
How It’s Made
One of the most common ways of making steel resist rust is by combining (alloying) it with a metal that is less likely to corrode: zinc. When steel is submerged in melted zinc, a chemical reaction permanently bonds the zinc to the steel. Therefore, the zinc isn’t exactly a sealer, like paint, because it doesn’t just coat the other metal; it actually permanently becomes a part of it. The most external layer is all zinc, but successive layers are a mixture of zinc and iron, with an interior of pure steel.
This process, known as hot-dipped galvanization, is one of the most common methods of making galvanized steel, but it’s not the only one. Continuous sheet galvanizing runs a steel sheet or wire through molten zinc; it’s also a form of hot-dipping, but leaves a thinner layer of the protective metal. Steel can also be painted or sprayed with zinc, although neither method creates the strong bond that hot-dipping does. Electrogalvanizing or electroplating uses electricity to create the bond between the two metals, which results in relatively thin layer of zinc.
The degree of galvanizing is usually described as the zinc’s weight per surface area rather than its thickness, because this gives a better representation of how much metal has been applied. Steel often gets galvanized after individual parts have been formed, such as braces, nails, screws, beams, or studs. Continuous sheet galvanizing is often done before the metal is used to create products, however, and can withstand some bending and forming without flaking.
Benefits of Galvanization
Zinc protects steel in two ways. First, it is highly resistant to rust; iron, a major component of steel, reacts very easily with oxygen and moisture and will eventually disintegrate. The layer of zinc on the surface prevents those elements from reaching the steel so quickly. It also develops a patina — a layer of zinc oxides, salts, and other compounds — that offers further protection. Zinc is also extremely durable and scratch resistant, and has a satiny appearance that many find attractive.
The outer layer also protects the steel by acting as a “sacrificial layer.” If, for some reason, rust does take hold on the surface of galvanized steel, the zinc will get corroded first. Even in areas where the surface is scratched or damaged, the surrounding zinc will still corrode before the steel does. The lifespan of galvanized steel varies, but industrial steel with a 3.9 mil (0.0039 inches or 0.09906 mm) thick coating can last more than 70 years without maintenance under average conditions.
Uses
Galvanized steel can be found almost everywhere. Many individuals live in steel frame houses, and buildings are often made with galvanized steel roofs. There are multiple steel parts in cars that help protect them from the weather, and it’s used in many marine applications due to its ability to withstand the salt and the elements. Besides being inexpensive, durable and effective, this metal is also popular because it can be recycled and reused multiple times.
Disadvantages
There are relatively few disadvantages to galvanization, but it’s not a good method for protecting all steel items. Some objects cannot be hot-dipped, often because they are too large or too small, and other forms of galvanizing often are not as protective and long-lasting. Eventually, the zinc will be corroded, although how long this takes depends on the thickness of the coating and the environment. Galvanized steel has a much shorter lifespan when it’s regularly exposed to rain or seawater.
Galvanized steel that is cooled too slowly or stacked together before they have cooled completely can also have the outer zinc layer peel away. In some cases, small gaps can form between the zinc and the underlying alloy, which can also cause peeling. When a very thick coat of zinc is applied, it can also become brittle and flake off.
Alternatives to Galvanization
Some metal items cannot be galvanized effectively; the coating of zinc would be too thick on a small screw, for example. In many cases, stainless steel, made with chromium, is used instead. Unlike galvanized metals, stainless steel is not coated in the metal; chromium is part of the composition of the steel alloy.
อ้างอิง:http://www.wisegeek.com/what-is-galvanized-steel.htm#comments

